Bentuk molekul dan gaya antar molekul
- BENTUK MOLEKUL
- Bentuk Molekul Berdasarkan Teori VSEPR
Bentuk molekul didasarkan kepada jumlah electron yang saling tolak-menolak disekitar atom pusat yang akan menempati tempat sejauh munkin untuk meminimumkan tolakan.
- Jenis pasangan electron disekitar atom pusat


- Symbol – symbol dalam teori VSEPR
- A : Atom pusat
- X : Jumlah pasangan electron ikatan
- E : jumlah Pasangan electron bebas
Catatan : ikatan rangkap dua atau rangkap tiga dihitung satu pasang electron ikatan
Bentuk-bentuk molekul sesuai dengan tipe molekul
1. Molekul linear

Tipe molekul : AX2
Contoh senyawa: CO2, BeCl2
2. Molekul segitiga planar atau segitiga datar

Tipe molekul AX3
Contoh molekul : BF3, NO3-, SO3, …
3. Bentuk molekul planar bentuk V

tipe molekul AX2E
contoh molekul SO2
4. Bentuk mlekul tetrahedral

Tipe molekul : AX4
Contoh molekul : CH4, CCl4,
5. Bentuk molekul trigonal pyramid

tipe molekul AX3E
contoh molekul NH3
6. Bentuk molekul bentuk v

tipe molekul AX2E2
contoh molekul H2O
7. Bentuk molekul trigonal bipiramid

tipe molekul AX5
contoh molekul PCl5
8. Bentuk molekul jungkat jungkit

Tipe molekul : AX4E
Contoh molekul :
9. Bentuk molekul bentuk T

tipe molekul AX3E2
contoh molekul IF3, BrF3
10. Bentuk molekul linear

Tipe molekul AX2E3
Contoh molekul : XeF2,
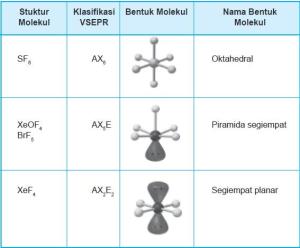
11. Bentuk molekul pyramid segiempat

tipe molekul AX5E
Contoh molekul : BrF5, XOF4,
12. Bentuk molekul octahedral

Tipe molekul AX6
Contoh molekul : SF6,
13. Bentuk molekul segiempat planar

tipe molekul AX4E2
contoh molekul XeF4,
Cara meramalkan bentuk molekul dengan teori VSEPR
- Tentukan struktur lewis dari rumus moleku
- Tentukan jumlah PEB dan PEI atom pusat
- Prediksi besar sudut ikatan dan arah yang munkin akibat tolakan
- Gambar bentuk molekul dan beri nama sesuai dengan jumlah PEI dan PEB
- Contoh soal 1
Penyelesaian
Molekul BeCl2
Struktur lewis BeCl2

Molekul NH3

molekul COCl2
struktur lewis

bentuk molekul

2.Bentuk Molekul menurut Teory Hibridisasi
yaitu bentuk molekul yang didasarkan kepada bentuk orbital kulit terluarnya, dimana terjadi pengabungan beberapa orbital membentuk orbital yang baru yang tingkat energinya sama yan disebut dengan hibridisasi.
Pembentukan orbital hibrida dapat dilihat dari conntoh berikut
molekul PCl5

Molekul CH4

molekul SF6


Bentuk-bentuk molekul berdasarkan teori hibridisasi

- Gaya antar Molekul
- 1. Gaya van der Waals
Gaya van der Waals dapat terjadi pada molekul-molekul polar dan molekulmolekul
nonpolar. Pada molekul-molekul polar disebut gaya dipol-dipol, sedangkan
pada molekul nonpolar disebut gaya dispersi (London).
a. Gaya Dipol-Dipol
Pada molekul hidrogen klorida, terjadi ikatan kovalen dengan struktur Lewis
sebagai berikut.

Atom klor lebih elektronegatif daripada hidrogen maka pasangan elektron
cenderung tertarik oleh Cl. Molekul HCl jadi memiliki dipol.
Hσ+ — Clσ+
Dua molekul yang masing-masing memiliki dipol akan selalu tarik-menarik dengan posisi bagian (–) berdekatan dengan bagian (+)
Gaya dipol-dipol pada asam klorida HCl dapat digambarkan

Gaya dipole-dipol pada molekul CH3Cl dapat ditinjukan pada gambar berikut

- a. Gaya Dispersi (Gaya London
Terjadinya gaya London dapat digambarkan oleh gambar berikut

A. Molekul Cl2 yang nonpolar
B. Dipol sesaat terjadi antar Cl2 yang berdekatan
C. Susunan molekul-molekul Cl2 yang terjadi karena gaya London
Gaya London pada molekul non polar
Gaya London sangat lemah, dan akan bertambah jika jumlah electron dalam molekul bertambah banyak.akibatnya titik didih makin tinggi.
1. Ikatan Hidrogen
Ikatan hydrogen adalah ikatan antara atom hydrogen dengan unsur yang sangat elektronegatif yaitu unsur F, O, N . hal ini tercermin dari kenaikan titik didih yang mencolok pada senyawa tersebut misalnya pada NH3, H2O. seperti gambar berikut
a. Ikatan hydrogen pada molekul air

Grafik titik didik hidrida pada gol VI A

Ikatan hydrogen pada molekul air
b. Ikatan Hidrogen pada molekul HF
Ikatan ini terjadi karena atom F jauh lebih elektronegatif disbanding atom H.
Perhatikan gambar berikut

Dari grafik-grafik tersebut yang menggambarkan titik didih hidrida golonganVA, VIA, dan VIIA terlihat bahwa NH3, H2O, dan HF mempunyai titik didih yanglebih tinggi dari hidrida yang segolongannya. Hal ini disebabkan oleh adanya ikatan hidrogen di antara molekul-molekulnya.